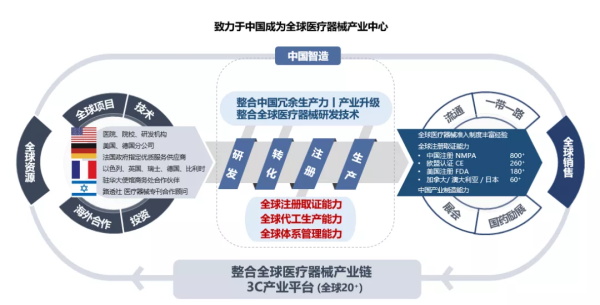
医疗器械是什么?奥咨达给出了一个浅显易懂的奥氏定义:“在医院里,除了人和药品,都是医疗器械”。医疗器械涉及材料、机械、电子、软件、声光等多行业,是一个多学科交叉、知识密集型的高新技术产业,使用于疾病治疗的全过程。中国人均医械费用远低于发达国家水平,高端产品逾八成依赖进口。随着居民健康消费升级,市场长期保持两位数增长,2020年将达到了8000亿,未来更有近三万亿的市场规模。
中国医疗器械企业数量众多,存在小、散、弱、新的特点,冗长的产业链和严格的合规要求带来了高门槛和运营成本,导致投资成功率偏低,企业获得一张二类产品注册证书需花费近3年,投入1到2千万,造成大量人力、土地和资金浪费。国内几百家医疗器械产业园的发展一直裹足不前,仅有厂房和资金并不足以支撑医械产业的持续发展,医工转化、科研转化的痛点亟需破解。
依托“健康中国2030”国家战略,中央办公厅和国务院办公厅发布的“医疗器械审评审批改革”中‘医疗器械注册人制度’的实施,生产许可证和注册证的分离,技术持有人无需自建厂房,不仅可以委托不同企业生产,还可以委托研发、委托注册、委托销售和技术转让,国产医疗器械产业发展迎来了全面加速期。
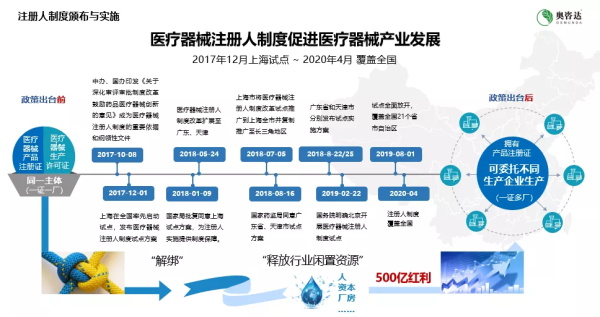
奥咨达历经近二十载的稳健发展,服务全球医械企业超过三千家,包含70%的中国医械上市公司和40%的世界500强医械企业。累计在全球取得医械证书过千张,其中欧盟CE300余张(占欧盟获批证书的10%)、美国FDA200余张、中国NMPA900余张。作为全球领先的医疗器械产业服务商,奥咨达一直伴随中国医疗器械法规发展历程,2018年4月,为承接医疗器械注册人制度,助力创新转化,打造医疗器械产业生态圈,全球首创产业模式“Cloud医械云 + CDMO研发制造 + CRO 高端服务” - 医疗器械3C产业平台诞生!创新的全产业链服务包括建设3C产业平台、提供产业服务(专业技术服务、云服务、金融服务等)、运营产业空间,为全球医疗研发者、企业、政府提供全方位、一站式的医疗器械产业解决方案。
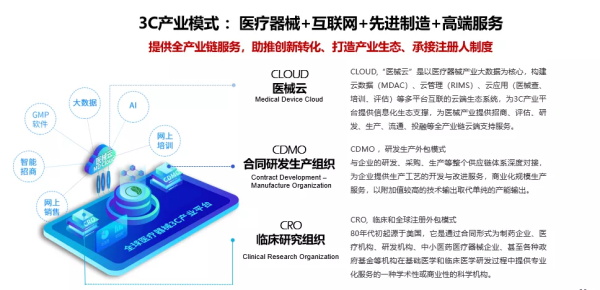
3C平台采用了产业资源共享模式,共享设备、人员、管理软件、空间、法规,包含无源器械、有源器械、诊断试剂专业生产线、医械云质量管理软件、10多个独立的检验检测中心和专业实验室、200多台高端检验和生产设备、标准仓储空间,可以同时满足100-300家医械企业的设计研发与生产需求,节约了大量的土地资源。在注册人制度下,二类产品通过3C产业平台委托生产,仅需服务费用100万,1年即可取证。取证成本下降90%,时间节约60%。时间等同于客户的财富,在疫情最严峻时刻,奥咨达仍不懈怠,竭力为一线抗疫提供多方面的专业力量(包括出口企业名单审核、钟南山基金会物资捐赠、免费法规咨询、应急产品注册等),同时为客户跟进各项服务,并于2020年5月,奥咨达取得全国第三方服务平台的首张注册证。

3C创新模式解决了产业中的三大需求和痛点。首先医生、科研人员、创业者、海外产品、创新产品等,希望低成本、高质量落地、快速取得医疗器械注册证书的需求;第二,已经获得医疗器械注册证书,生产规模较小,希望节省成本,迅速扩大市场的医械小微企业需求;第三,拥有相关资源,希望进入医疗器械大健康产业的政府、园区、企业、地产、资本等的需求。同时,根据企业不同时期的资本需求,2019年,奥咨达携手中国银行推出了“中银奥贷”普惠金融产品,并与专业基金合作,解决了医疗器械创业者们融资难、贷款难的问题。
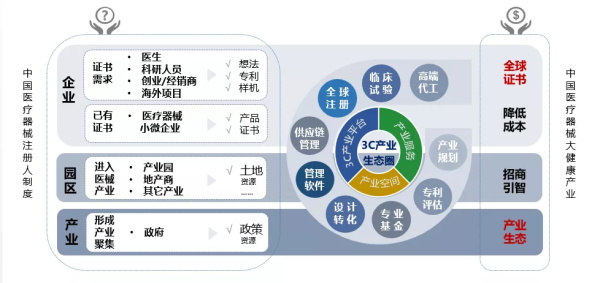
奥咨达借助北、上、广、深四大超级城市在医院、科研院校、海量资本、双创人才的聚集优势,创建了3C产业平台,同时与国内省会城市、园区、合作伙伴紧密合作将在各地筹建,未来拓展至美国、欧洲、以色列、日本等全球医械技术集聚地,为高端医疗器械的海外引进、科研转化、规模生产提供强有力的平台支撑。基于3C产业平台的医疗器械产业生态,其规模可因需建设为几百平方米的医疗器械创新中心、或几万平方米的专业孵化器和加速器、甚至几十万平方米的专业产业园和健康小镇。为实现3C平台的标准化、产业化、专业化、品牌化与国际化,医械云的质量管理软件RIMS将全球管理标准(ISO13485、GMP、QSR820)、监管法规和奥咨达三千多家企业的服务经验等内容融入系统,将工厂管理、工艺流程、表单记录等管理程序标准化处理,使全产业链服务更体系化与数据化。
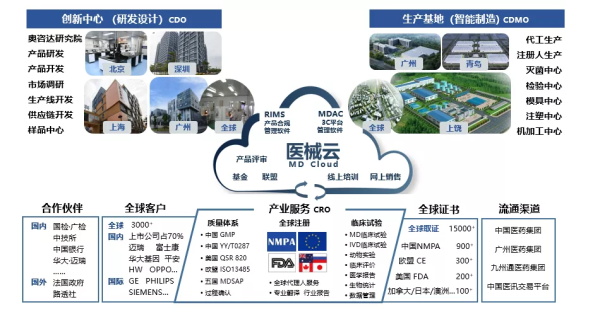
3C产业模式推动了产业、人才、技术、法规、资本的聚集,助力国内外创新成果转化落地,加速产业整合发展与技术升级,同时降低政府的监管风险,提高土地、资本的使用效率。3C产业平台将成为企业成长的助手、政府招商落地的帮手、产业发展的推手。医疗器械是关系国计民生的支柱产业,也是培育发展战略新兴产业的重点领域。奥咨达怀揣“中国成为全球医疗器械产业中心”的理想,通过“建设3C产业平台、提供产业服务、经营产业空间”的运营模式,向全球输出顶级的中国服务和医疗器械,让医疗器械成为中国新名片的闪亮组成部分。