根据工业和信息化部发布的数据,“十三五”期间,我国医疗装备产业实现快速发展,市场规模从2015年的4800亿元增长到2020年的8400亿元,年均复合增长率11.8%;制造体系基本健全,形成了22大类1100多个品类的产品体系,覆盖了卫生健康各个环节;企业主体发展壮大,形成了一批具有较强竞争力的龙头企业。截止到2021年,我国已成为全球重要的医疗装备生产制造基地。
在国家政策鼓励创新医疗器械国产化的大背景下,我国医疗器械产品正逐步从中低端市场向高端市场实现升级,国产化进程不断加深,国产医疗器械迎来了黄金时代。面对行业风口,不少企业纷纷加入国产化医疗器械赛道。为了加快上市进程,医疗器械生产企业逐渐倾向于将项目委托给更懂医疗器械产品、更懂医疗器械法规、更懂医疗器械项目管理的专业CRO公司进行临床试验及注册等工作,而且医疗器械生产企业已不满足常规流程化技术服务,他们更需要能够提供定制化、规范化、信息化服务的智囊团。这为国内CRO企业带来广阔市场的同时也提高了CRO行业入门门槛,是机遇也是挑战,信息化时代,谁掌握了大数据,谁才有可能成为赢家。

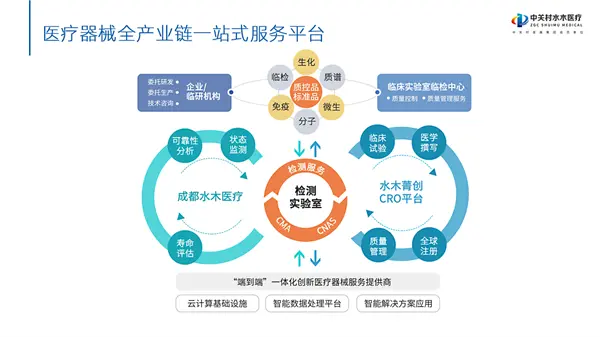
北京水木菁创医药科技有限公司(下称“水木菁创”)是一家专注于为医疗器械企业提供专业临床研究技术服务的合同研究组织(CRO),主要为医疗器械(含体外诊断试剂)企业提供医疗器械临床试验、医学撰写、全球注册、GMP咨询等专业化技术服务与一站式解决方案。其所在的中关村水木医疗技术集团是集“工程化研发+检验检测+体系建立运行辅导、临床试验+注册”于一体的全产业链一站式服务平台。多年深耕精研,多年专业领域法规研读,多年医疗器械标准、法规参与制定和修订,拥有丰富经验和多项荣誉的同时也收获了各领域医疗器械大数据信息,而今,中关村水木医疗技术集团已在行业内具有相当影响力。
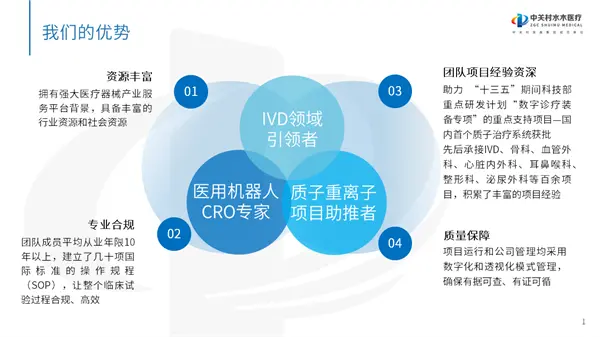
目前,水木菁创公司员工百余人,拥有一支具有超强学习能力、应变能力、国际专业水准、高素质的研究服务团队,核心管理层均来自国内外知名制药企业、医疗器械企业、CRO的行业精英,平均从业年限在十年以上,建立了几十项国际标准的操作规范(SOP)。团队精通各类医疗器械法规咨询技术服务,参与过众多项目的执行与策划,对医疗器械行业有着丰富的政策法规积累和实践经验。
水木菁创CRO平台,筑造国产护城河
医疗器械临床试验是一项高技术、高风险、高投入和长周期的复杂系统性工程,每一项临床试验、注册申报都需要经历临床试验方案设计、多中心选择、临床评价资料编写等不同阶段。大部分中小型医疗器械企业规模小、产品种类单一、团队尚未完善,漫长的临床试验周期,需花费大量的时间成本、资金成本、还有人力成本。因此,与熟悉法规、专用性强的CRO机构合作,能有效缩短项目研究周期、降低项目失败的风险,加快上市流程,抢占时机,实现产品盈利。
水木菁创CRO平台通过自身优势,专注于为医疗器械企业提供优质、高效、便捷、精准的一站式产品上市解决方案,致力于为中国医疗器械研、检、产、商提供专业支持。在专业平台加持下,水木菁创通过资源整合的优势,丰富的项目经验和专业化的服务大大缩短临床试验周期,提高项目推进效率,为产品上市提速,助力国产化医疗器械产业发展。
多项成果加身,实力助推发展
经过多年的沉淀,水木菁创在医疗器械临床试验方面有着扎实的技术积累,在技术人才、技术水平、质量控制、业务经验、行业资质和客户资源等方面已具备较强优势。自成立以来,公司先后为近千家医疗器械企业提供法规咨询技术服务,且以创新、高风险等具有挑战性的医疗器械为主,形成了长期稳定的合作关系。目前,公司正在运行的项目涵盖医疗器械有源、无源和IVD领域等,聚焦国产医疗器械临床试验发展,团队经验丰富,累计取得注册证超过1080张,涉及国内外相关领域。
在今年1月份,水木菁创助力申办方,斩获中国首张国产膝关节置换手术机器人注册证,实现了国产膝关节手术机器人“零的突破”。另外,水木菁创承接的国内首台髋膝关节置换机器人产品也顺利获批,两项脊柱外科手术机器人顺利取证。截至目前,水木菁创已经在各类手术机器人项目积累了大量经验,涉及康复科、骨科等,涉及的方向包括康复机器人、骨科手术导航定位系统、膝关节手术导航系统、髋关节假体系统、手术机器人定位系统、采血机器人、手术机器人麻醉机/无创呼吸机多款手术机器人等。
不仅如此,水木菁创不断推进IVD产业链布局,助力体外诊断产业发展。IVD事业部团队成员均拥有多年医疗器械临床试验方案设计及医学撰写经验,涉及生化类、免疫类、分子诊断类等在内的多个治疗领域IVD产品;同时,团队成员定期接受培训,熟悉IVD产品注册相关法规,能够及时捕捉当下新法规动态和行业详情,并形成一套具有独特见解、科学严谨的规划思路,以确保递交的文档质量。在2020年初,水木菁创率先完成了2个新型冠状病毒(2019-nCoV)抗体检测试剂盒(量子点荧光免疫层析法、酶联免疫法)的应急批件申请,并为几十家企业提供前沿的应急法规解读咨询服务。目前,水木菁创还有8个新型冠状病毒(2019-nCoV)抗原检测试剂盒的临床项目在进行中。随着水木菁创在IVD领域临床试验的不断发展,高水准的服务治疗和高效省时的资源平台整合能力,为客户提供全方位一体化服务,使客户更省心、更满意!

水木菁创助推医疗器械临床试验发展,除了在手术机器人、IVD领域持续深耕,在国之重器—质子治疗领域也处于引领地位。9月26日,水木菁创助力国产首台质子治疗系统获批上市,该项目由水木菁创提供全流程临床试验及注册服务。在今年8月初,水木菁创承接的另一质子治疗临床试验项目,随着最后一例患者完成治疗出院,意味着水木菁创再次协助申办方顺利完成了临床试验治疗阶段工作,标志着又一“国之重器”即将进入国家药监局注册审评审批阶段。水木菁创在质子治疗的注册和临床试验方案上有着深厚的理论基础和丰富的实践经验,为申办方提供实用高效的医学方案设计思路。面对质子治疗临床试验的严苛标准,水木菁创始终迎难而上,勇于挑战,积极又谨慎,做到临床试验每个环节都科学、合理、稳妥,精准把控关键流程项目管理,遵照相关医疗器械法规要求撰写、辅导、整理、搜集相关文献、文件并汇总所有注册文件,助力申办方取得注册证!
善为、敢为、勤为、有为。多年来水木菁创一直十分重视医疗器械临床试验工作,不忘初心,积累了大量的技术知识储备。作为一家高新技术企业,公司通过不断地努力和自我超越,获得了中关村国家自主创新示范区高精尖产业创新平台、软件著作权登记证书、ISO 9001:2015质量管理体系认证等荣誉,未来也将继续往行业顶尖方向迈进,助力医疗器械国产化的进步与发展。
下一篇:创新,美敦力又下一城